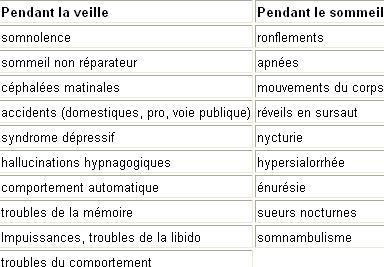
Aspects cliniques du SAOS Le SAOS est responsable de plusieurs manifestations cliniques :
 Ronflement
RonflementTrès fréquent dans la population générale.
Interrogatoire peu fiable (y compris l’hétéro-anamnèse). Moins reconnu par les sujets jeunes.
La prévalence est estimée a 60 % des hommes et 40 % des femmes. Augmente dans les deux sexes après 35 ans, mais diminue chez l’homme après 65 ans. Le ronflement du SAOS est souvent intense, interrompu par des apnées (silence) avec une reprise « explosive » qu’accompagnent des mouvements des jambes.
Mais il existe des SAOS sans ronflement (grande insuffisance respiratoire, patients opérés)
ApnéesPas toujours perçues par le patient, source d’inquiétude pour le conjoint. Responsable de réveils en sursaut avec sensation d’étouffement.
Sueurs nocturnes dans 66 % des cas
Somnambulisme dans 10% des cas. Sensation d’insomnie pouvant générer une prescription d’hypnotiques aggravant le SAOS
Nycturie présente dans 28 % des cas (par probable sécrétion de facteur natriurétique auriculaire provoqué par les apnées et la dépression thoracique).
Trouble de la libido retrouvés chez 28 % des patients.
Somnolence diurne par déstructuration du sommeil et disparition des phases de sommeil profond. Manifestations post-prandiales puis en l’absence de stimulation (réunion, conduite, en lisant…). Évalué par l’échelle de somnolence d’Epworth. Parfois sous-estimées par le patient car ancienne et banalisée. Parfois associée à des comportements automatiques (rasage long, …)
Troubles du comportement irritabilité et agressivité , dépression, troubles cognitifs, céphalées matinales. Il faut rechercher, par l’interrogatoire,des antécédents de réveils post-opératoires compliqués (extubations difficiles, réanimation post-opératoire) ,
une HTA , une pathologie obstructives, des interventions ORL, une prise de médicaments.
Échelle de somnolence d'Epworth La probabilité de s’endormir est cotée de 0 à 3 selon le risque d’assoupissement
0 = jamais d’assoupissement
1 = risque faible d’assoupissement
2 = risque modéré d’assoupissement
3 = risque élevé d’assoupissement.
Elle est évaluée pour huit situations différentes:Assis en train de lire
En regardant la télévision ;Assis, inactif, dans un lieu public ;Comme passager dans une voiture roulant pendant 1 heure sans s'arrêter;Allongé pour se reposer l’après-midi quand les circonstances le permettent
Assis en train de parler à quelqu'un;Assis calmement après un repas sans alcool
Au volant d'une voiture immobilisée quelques minutes dans un encombrement
Le total est noté sur 24
Un score > 12 : somnolence pathologique.
Chez qui demander une enregistrement polysomnographique ?Les éléments cliniques les plus pertinents sont :les ronflements, les apnées décrites par le conjoint, la somnolence diurne excessive,
la surcharge pondérale (IMC > 27 kg/m²) l’âge, le sexe masculin, les antécédents familiaux,
l’HTA.
Aucun de ces éléments n’est très spécifique. Les apnées retrouvées chez 65 à 92 % des SAOS mais aussi chez 31 à 64 % des sujets normaux.
L’absence de somnolence diurne estimée ( Epworth< 12) n’exclut pas le SAOS (40 % des SAOS ?).
Le score d’Epworth n’est pas liés a la sévérité du SAOS.
Il existe une meilleure sensibilité en associant ronflement et somnolence diurne.
L’obésité (la plus souvent androïde) est un facteur de risque de SAOS (80 % des SAOS sont obèses).
Mais l’obésité, seule, a une faible valeur prédictive de SAOS.
Des scores avec âge, IMC, périmètre du cou, présence d’apnées et ronflements, HTA ont été élaborés ; plus sensibles (92 %) mais peu spécifiques ( 51%) ils permettent un dépistage des SAOS.
Ces résultats n’ont été validés que dans des populations restreintes.
Des critères morphométriques ont été utilisés (mesures de la cavité buccale, BMI , tour de cou) augmentant la spécificité sans permettre pour autant l’élimination de la Polysomnographie.
Polysomnographie C’est un enregistrement au cours d’une nuit (voire d’une sieste pour le dépistage) de sommeil, visant à quantifier les évènements respiratoires (apnées, hypopnées ) et à les corréler à des variables que sont :
le stade de sommeil et les micro-réveils; par enregistrement d’EEG, (électrodes de scalp), d’un électro-oculogramme (électrodes collées à l’angle externe de l’œil) et d’un EMG (électrodes collées sur le menton)
la position du sujet : par des capteurs décelant les réactions aux évènements respiratoires et la position de survenue de ces évènements.
les efforts respiratoires :par des sangles abdominales et thoracique avec des capteurs sensibles à l’étirement. Des mesures plus fines nécessitent l’utilisation d’une sonde de pression œsophagienne.
les répercussions gazométriques : par mesure de la saturation en oxymétrie percutanée
les répercussions cardio-vasculaires : avec la mesure de la fréquence cardiaque(la mesure de la TA n’est pas faite en routine).
La mesure des flux ventilatoires met en évidence les évènements respiratoires : ils peuvent être analysés par enregistrement de la température à la bouche et aux deux narines.
Ces mesures dépistent les apnées mais plus difficilement les hypopnées : leurs dépistages reposent sur la modification de signal thermique associé le plus souvent à une désaturation ou à un micro-réveil.
Le pneumotachographe reste la méthode de référence pour la mesure des flux ventilatoires.
Pour alléger ces dispositifs des polysomnographies « partielles » ont été proposées. Cela va de la seule recherche de désaturation nocturne (publications contradictoires) a un examen sans enregistrement des stades du sommeil (sans EEG, EMG ni electro-oculogramme).
Cette technique peut-être suffisante si elle est positive mais ne permet pas de déceler les micro-réveils.
Enfin certaines équipes font de la PSMG ambulatoire avec le risque de défaillance en l’absence de technicien.
TraitementDe multiples traitements du SAOS ont été évalués :
mesures hygiéno-diététiques (perte de poids, arrêt de la consommation d’alcool ou de sédatifs) ; une efficacité incomplète et transitoire.
traitements positionnels visant à empêcher le décubitus dorsal au cours du sommeil (efficaces chez une petite fraction des patients seulement) ;
application nocturne d’une pression positive continue (PPC) par voie nasale ;
trachéotomie ; constamment efficace
autres traitements chirurgicaux
traitements médicamenteux (antidépresseurs stimulants dont les tricycliques,…)
traitements instrumentaux (Orthèse d'avancée mandibulaire, sondes d’intubation naso-trachéale, dilatateurs narinaires).
Ventilation en pression positive continue (PPC) Le traitement de référence reste la ventilation en pression positive continue.
Elle maintient ouverte à tous les stades du cycle respiratoire les voies aériennes supérieures.
Elle semble aussi en partie efficace sur les apnées centrales.
PPC simple : l'appareil délivre le même niveau de pression lors des phases inspiratoires et expiratoires et ce durant toute la nuit.
PPC avec relachement de pression à l'expiration (C-Flex® Respironics, iSleep 20+ eAdapt Breas) : Réduction de pression au début de l'expiration afin de réduire la gène expiratoire.
PPC auto-pilotée : adaptation spontanée aux besoins de pressions au cours de la nuit variables (position de sommeil, stade du sommeil, réduction d’adaptation en début de traitement, médicaments ou alcool, etc.). Réglé autour d’une pression de référence.
Pression Positive à double niveau de pression (BiPAP® Respironics, iSleep 25 Breas) : l'appareil délivre une pression moindre à l’expiration et plus forte à l'inspiration pour favoriser le confort respiratoire.
Pression Positive à double niveau de pression auto-pilotée (BiPAP® Auto Respironics) : les 2 pressions sont automatiquement ajustées au cours de la nuit selon les besoins du patient
Les appareils délivrent des pressions de 3 à 20 cm H2O à des débits de 20 à 60 l/min.
L’appareil pèse de 1 à 2 kg, son bruit de varie 25 - 30 dB.
Les masques sont très variés, en silicone ou en gel avec dispositif de maintient (sangle, harnais, …).
Il faut une « fuite calibrée » pour éliminer le CO2.
Le calibrage des pressions de ventilation se fait au cours d’un deuxième enregistrement PSG en débutant en début de nuit par des pressions faibles progressivement augmentées par paliers de quelques minutes pour faire disparaître les apnées, les hypopnées, les « événements respiratoires » et les ronflements.
Cette première nuit est importante car elle permet parfois un sommeil de qualité, vécu comme réparateur avec régression de la somnolence diurne, elle est un bon critère pronostic de compliance à la PPC.
À long terme, l’efficacité dépend de l’observance. Le taux initial d’acceptation est de 70 à 80 %, avec un maintien à 80 % à distance mais avec des durées d’utilisation variable (« mouchards » dans les appareils récents) ; la durée minimale efficace est de 5 h par nuit.
L’observance dépend de la prise en charge et de l’information des patients, et en particulier de la gestion des effets secondaires mineurs de la PPC :
Irritation cutanée par un masque inadapté,
Rhinite voire obturation nasale (humidification chauffante),
Conjonctivites par fuites du masque (bruit peu souvent évoqué).
La PPC peut avoir des effets secondaires plus importants : épistaxis, pneumothorax, trouble du rythme cardiaque.
Les principaux bénéfices concernent l’amélioration de la vigilance diurne, mais certaines études font état d’une réduction de la mortalité, d’une baisse des accidents de la route.
L’amélioration de l’HTA est controversée.

